2000 年諾貝爾生理或醫學獎 無殼蝸牛立大功
黃頂立 DEENG-LIH HUANG, Ph.D.
美國哥倫比亞大學生物有機化學博士
E-mail: dh459@columbia.edu
(電腦字數統計:中文字 4,682,英數字 187。附 4 個圖和 4 個小附文)
無殼蝸牛歷經長期的犧牲奉獻後,在
2000 年 10 月 9 日終於可以感到特別榮耀,因為在那一天, 2000
年諾貝爾生理或醫學獎公佈了,無殼蝸牛正是得獎的大功臣之一。
2000 年諾貝爾生理或醫學獎由瑞典哥生堡 (Gothenburg) 大學的名譽退休教授卡爾生 (Arvid Carlsson,77
歲)、美國紐約市洛克斐勒大學的葛林加德 (Paul Greengard,74
歲) 和紐約市哥倫比亞大學的肯德爾 (Eric Kandel,70 歲) 三人共同獲得。根據諾貝爾獎評審會的頌詞,他們是因為在有關「神經系統的訊息轉導」(signal transduction in the nervous system) 的研究發現而獲獎。
這三位得主是在他們的研究領域都是名符其實的大師。其中我的母校哥倫比亞大學的肯德爾更是跨越多個領域、早享譽盛名的一代開山宗師,他開啟了神經科學中的學習和記憶領域做細胞分子層次研究的大門,而且不斷的做出領導性和突破性的研究,即使今年他已
70 歲,他目前的研究還是走在這個領城的最前端。他早在 1983
年就獲得最被人垂涎、素有「美國的諾貝爾獎」盛名之稱的「亞伯雷斯克獎」(Albert Lasker Award,見附文
1) 的基礎醫學研究獎,早就被看好排隊在等著拿諾貝爾獎。同時,他早在
1983 年也成為哥倫比亞大學學術地位最祟高的「大學教授」(University Professor)。哥大鼓勵「大學教授」做跨越領域的研究,目前哥大有九位「大學教授」,其中包括得過諾貝爾物理獎的李政道和我的博士研究指導教授
Ronald Breslow。我的指導教授 Breslow 也是早就排隊在等諾貝爾獎的人,曾告訴過我們,「大學教授」享有的殊榮之一,就是可以在任何學系開任何喜歡開的課,即使是從來沒有的課。
卡爾生 (Arvid Carlsson)
卡爾生獲獎是因為在 1950 年代末期,發現多巴胺 (dopamine) 是腦部的一個神經傳導因子及多巴胺對控制身體的動作十分重要。
在那個時代,多巴胺被認為只是合成另一個神經傳導因子正腎上腺素的一個前驅物(圖一)。他研發出一個具高敏感度的方法,可以分析多巴胺的量,結果發現多巴胺的量在腦部的某些區域,比正腎上腺素的量還要高,於是他推斷多巴胺本身也是一個神經傳導因子。腦部多巴胺的量特別高的區域是在基底神經節
( basal ganglia)。
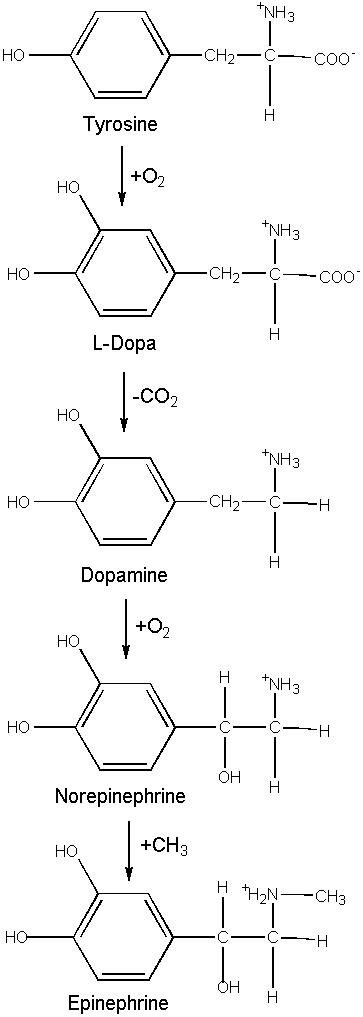
圖一:多巴胺、正腎上腺素和腎上腺素都是神經傳導因子。體內合成這些神經傳導因子的步驟,首先是一個反應速率控制的步驟,由酪胺酸 (tyrosine) 氫氧化成
L-多巴 (L-dopa);接著L-多巴失去二氧化碳形成多巴胺 (dopamine);多巴胺再氫氧化就生成正腎上腺素
(norepinephrene);正腎上腺素可以再進一步甲基化變成腎上腺素
(epinephrene)。這些反應步驟都需要酉每的催化。
可降血壓的天然藥物利血平 (reserpine)
可以減耗一些神經傳導因子在「突觸」(見圖二說明)的貯存量。卡爾生做了一系列的實驗,施予動物利血平後,動物就失去了自然的動作能力。當他再施予
L-多巴後,動物又可恢復自然的動作能力。他還顯示用 L-多巴治療,可以使腦部多巴胺的量變成正常。
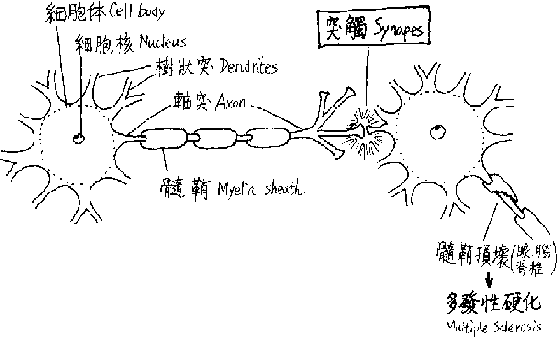
圖二神經細胞的構造:如果一個神經細胞價值一塊錢,猜猜看你的腦袋價值多少錢?哇!發了!發了!你發了!超過一千億元!是的,人的腦袋裡有超過一千億個神經細胞。神經細胞有各種不同的形狀和大小,圖一顯示典型的神經細胞構造。神經細胞的構造有細胞體,其中間有個細胞核。細胞體周圍有許多個樹狀突和一個軸突;顧名思義,樹狀突長得像樹枝的形狀,較短;軸突則長得像條主軸,所以較長。軸突可以將訊息由細胞體送出,傳遞給另一個神經細胞的樹狀突接收,再送入細胞體。不過軸突傳遞訊息到樹狀突時,兩者的末端並沒有接觸在一起,而是留有一個空隙,兩者的這個末端就叫做突觸 (synapses)。突觸是2000年諾貝爾生理或醫學獎有關「神經系統的訊息轉導」的一個重要部位。此外,軸突就好像電線,周圍有一節一節的髓鞘保護。如果髓鞘損壞,就會產生所謂的「多發性硬化症」(圖二右下角),通常發生在眼、腦和脊椎的神經細胞。
有沒有好奇為什麼要用 L-多巴,而不直接用多巴胺呢?原來是因為外來的多巴胺不能滲入腦部,而外來的
L-多巴可以滲入腦部,在腦部合成多巴胺(圖一)。
另外,卡爾生發覺利血平在動物身上所引發的症狀和帕金森氏症
(Parkinson's disease) 相似。他進一步研究,發現帕金森氏症病人腦部的基底神經節缺乏多巴胺。結果
L-多巴就被發展成為治療帕金森氏症的藥物,而且即使到現在,仍舊是最重要的標準治療藥物。至於為何基底神經節製造多巴胺的細胞會死亡的原因,至今仍不清楚。帕金森氏症腦部的多巴胺由基底神經節運送到額葉(大腦前方)異常。而額葉負責控制身體的動作,當額葉缺乏多巴胺時,會產生帕金森氏症的症狀,例如顫抖、肌肉僵硬、行動能力降低、失去臉部表情等。
精神分裂症 (schizophrenia,見附文 2) 是另一個和多巴胺有關的疾病,不過和帕金森氏症相反的,卻是和腦部多巴胺的過度反應有關。卡爾生發現治療精神分裂症的一些精神病藥物(例如在
1950年代就存在的第一個治療精神病的藥物 chlorpromazine,其長相請見圖三)降低症狀的作用機制,是可以阻擋多巴胺受體,因而降低多巴胺在突觸的傳導,所以就可以降低多巴胺的過度反應。
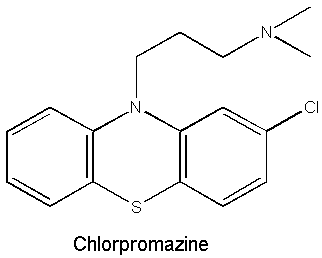
圖三:在 1950 年代就存在的第一個治療精神病的藥物 chlorpromazine
此外,注意力不足活動過度症 (ADHD, attention deficit hyperactivity disorder,見附文
3) 也是一個和多巴胺有關連的病症。雖然其病因還不清楚,一般認為和腦部多巴胺的活性不足有關。
卡爾生在腦部神經傳導因子作用機制的研究,對治療有關腦神經傳導因子的疾病的藥物研發有重大的影響。例如正腎上腺素和血清素便是和憂鬱有關的兩個主要神經傳導因子,當其量少時會憂鬱,而其量多時則會感覺快樂。新一代治療憂鬱較好的藥物 (如百解憂
prozac),是可以選擇性的阻擋血清素的再吸收,而維持血清素量的充足,所以可去除憂鬱。卡爾生在這些藥物的研發,也有重大的貢獻。
葛林加德 (Paul Greengard)
雖然人們在 1960 年代末期已經知道多巴胺、正腎上腺素和血清素是中樞神經系統的神經傳導因子,但是其作用機制卻還不清楚。葛林加德的貢獻,就是發現這些神經傳導因子在突觸的作用機制,尤其是發現蛋白質磷酸化在這整個步驟中扮演非常重要的角色;而且蛋白質磷酸化也發生在其他的生理反應(例如荷爾蒙的作用),其在作用機制上所扮演的,是共通的一個非常重要角色。
在那個時代,神經科學家大多熱門於神經電化學方面的研究,葛林加德卻勇於和別人不一樣,選擇冷門的蛋白質磷酸化做研究。結果他使這冷門的領域發光發亮變成熱門的重要領域。
神經傳導因子如多巴胺、正腎上腺素、血清素和某些神經月生月太
(peptides) 等,傳導訊息藉由所謂的「慢突觸傳導」(slow synaptic transmission),會導致神經細胞功能的改變,這改變可維持數秒到數小時。至於神經細胞功能之所以會改變,則非常重要的,是由蛋白質磷酸化所造成的。「慢突觸傳導」負責神經系統的一些基本功能,例如警覺性和心情。「慢突觸傳導」也可以控制「快突觸傳導」。「快突觸傳導」負責講話、動作和感覺等。
葛林加德發現當做第一信使的多巴胺和細胞膜的多巴胺受體結合後,會刺激腺甘酸環化酉每 (adenyl cyclase) 催化
ATP 製造環腺甘酸 (cAMP);cAMP
就和接力賽一樣變成第二信使,再活化蛋白質活化酉每
A (PKA、protein kinase A);接著蛋白質活化酉每
A 便催化磷酸加到蛋白質上的生化反應,也就是所謂的蛋白質磷酸化。神經細胞的蛋白質磷酸化後就會產生各種不同功能,其中重要的一類,是蛋白質磷酸化的離子管道,可以控制神經細胞對刺激的反應性,使神經細胞可以沿著突軸和末稍傳導電脈衝。
在神經細胞的磷酸化蛋白質中,葛林加德更進一步研究出一個具蛋白質磷酸化酉每-1 (protein phosphatase 1) 抑制劑功能、可調控其他蛋白質的龍頭老大,他稱之為
DARPP-32 (多巴胺和環腺甘酸控制的磷酸蛋白質、分子量 32,000,dopamine- and cyclic-AMP-regulated phosphoprotein of molecular weight 32,000)。DARPP-32
身為龍頭老大,當然一聲令下就可以指揮手下的小弟 -- 其他蛋白質
-- 做各種不同的功能。
葛林加德最新的研究,發現龍頭老大 DARPP-32 和杭亭頓氏病 (Huntington's disease,見附文
4) 也有關連。在 2000 年一月的美國國家科學研究院學報 (Proc Natl Acad Sci USA),葛林加德的研究團隊用導入杭亭頓氏病基因的老鼠研究,發現杭亭頓氏病症狀發生前的老鼠腦部紋狀體有嚴重的多巴胺信息缺乏,其中也包括龍頭老大
DARPP-32。
阿滋海默氏症 (Alzheimer's disease) 腦部有老化的 b-澱粉斑 (月生月太,
peptide) 沉澱,葛林加德也做有關磷酸化蛋白質如何調控 b-澱粉月生月太的作用機制的研究,這對發展治療阿滋海默氏症的藥物是很重要的。在
2000 年二月的美國國家科學研究院學報 (Proc Natl Acad Sci USA),葛林加德研究團隊的最新研究,顯示老鼠補充睪丸酮 (testosterone) 可降低神經細胞分泌
b-澱粉月生月太
(peptide) 30-45%。所以人類補充睪丸酮類物質是治療阿滋海默氏症的一個方向,不過還得考慮如何降低睪丸酮所可能引起的副作用。
肯德爾 (Eric Kandel)
肯德爾的研究和貢獻其實和前兩位不完全相同,肯德爾開創了一個跨越多個領域的全新科學領域,而且使其成為燦爛耀眼的重要領域。
肯德爾在哈佛大學時主修歷史和文學,同時也對精神病學發展出興趣,所以畢業後就到紐約大學醫學院修精神病學,準備以後成為精神病分析醫師。不過當他到醫學院時,他問他自己,什麼是精神病的核心議題呢?他體認到除了基因以外,記憶是最重要的。所以他決定朝腦部和記憶的方向發展。
腦部的海馬負責學習和記憶,所以他最初著重在腦部海馬的研究,包括他在美國健康研究院 (NIH) 時的博士後研究。但在那個時代,腦部海馬還不適合做嚴密的記憶研究。他想做的是細胞分子層次的研究,他想應該要選擇一個較簡單、神經細胞較大的動物著手,於是便大膽的選擇在動物王國裡神經線最粗的海蝸牛
Aplysia californica。
海蝸牛是無脊椎動物,神經細胞相對的少,只有約二萬個,有些可大到直徑 1 毫米 (mm) ,容易檢辨和容易測量其神經電位,及容易用電極或注射化學品實驗;同時,海蝸牛受刺激時,會產生一個簡單的保護性反射動作將鰓縮起來,所以適合做學習和記憶的作用機制基礎研究。海蝸牛長得像蝸牛,不過背上無殼,所以是天生的無殼蝸牛,其鰓就在其背部兩大片疣足包著的蓋穴裡,很容易觀察到。
海蝸牛是雌雄同體,陰莖在頭部右邊,陰道也是在背部疣足包著的蓋穴裡。海蝸牛經常是一群在一起生活,所以交配時常會出現一個很奇妙又有趣的畫面,就是會一隻接一隻的排排站,後面的一隻把頭塞到前面一隻的背部蓋穴裡埋頭苦幹,其中第一隻只當母的,最後一隻只當公的,中間的則同時當公的和母的。
海蝸牛的頭有兩根觸角,所以也被稱為海兔 (sea hare),不過這需要想像力的配合,因為其觸角實在是小的真不像兔子的耳朵。另外,海蝸牛也是章魚的親戚,所以也有忍無可忍就噴墨的功夫,小心噢!可不要隨便惹毛海蝸牛囉!
肯德爾果然很小心,不敢隨便惹毛海蝸牛,特別在 1962 年到法國巴黎跟海蝸牛專家
Ladislav Tauc 學習研究。當初他選擇海蝸牛來做腦部學習和記憶在細胞分子層次的研究實在是跌破專家的眼鏡。不過他所開創的這條新路,一路走來是成果豐碩、風光滿面的康莊大道,無殼海蝸牛真是他的大功臣。
肯德爾首先要教導海蝸牛學習受到那些刺激要將鰓縮起來,然後檢驗分析那些神經細胞參與反應,結果發現學習可以導致神經電位的改變。
學習的基本形式分成非關連性 (nonassociative) 和關連性 (associative) 二大類。非關連性學習有如 (1) 習慣
(habituation) -- 例如每隔一段時間重覆輕觸海蝸牛的尾部,在第一次輕觸時,海蝸牛以為具有傷害性,會產生保護性反射動作將鰓縮起來,同時突觸的神經電位也會變大。不過接下來幾次的重覆輕觸,海蝸牛已經學習到這樣的輕觸不具傷害性,所以會將其忽視而變成一種習慣,突觸神經電位也不再變大。(2) 導致過敏作用
(sensitization) -- 用有害的刺激,例如用電極刺激海蝸牛的尾部,讓其學習到這是需要害怕的刺激,其突觸神經電位會變大,鰓縮起來的保護性反射動作,則是隨著刺激的強度而維持數分到數小時。關連性學習有如典型的條件作用 (classical
conditioning) -- 用一個有害的刺激配對一個中性的刺激,讓海蝸牛學習到在這樣狀況的中性刺激也會產生害怕的反應,使其除了鰓會縮起來外,突觸神經電位也會變大。
肯德爾經由對海蝸牛學習和記憶的研究,探究出短期記憶和長期記憶的作用機制,其發生的地點都是在突觸。
較弱的刺激會形成短期記憶,其作用機制是和葛林加德發現的蛋白質磷酸化一樣,神經傳導因子血清素促進
cAMP 製造;cAMP 再活化蛋白質活化酉每
A (PKA);PKA 再使特定離子管道(如鉀離子管道)蛋白質磷酸化,結果造成這特定離子管道失去活性,而增加鈣離子進入神經末稍,導致神經傳導因子在突觸的釋放增加,因而造成反射作用的增強,就形成短期的記憶。
較強和較久的刺激會形成長期記憶,其作用機制前面幾步同樣是神經傳導因子血清素
→ cAMP → PKA → 蛋白質磷酸化,不過由於刺激較強和較久,這些步驟所增加的量都會大增,結果會影響到細胞核再合成新的蛋白質。細胞核合成新的蛋白質是和短期記憶不同的關鍵,可導致突觸的形狀和功能的改變,也就是所謂的「突觸可塑性」 (synaptic plasticity),因而可增強突觸的效能和神經傳導因子的釋放,而形成長期的記憶。
如何影響細胞核再合成新的蛋白質呢?肯德爾進一步的研究,發現一個新的蛋白質,稱之為
CREB (cAMP response element binding protein,cAMP
反應要素結合蛋白質),可活化細胞核的促進新蛋白質合成的一些基因。當把
CREB 阻擋住時,長期記憶便無法形成,所以 CREB 是將短期記憶轉換成長期記憶的關鍵蛋白質。此外,還發現另一個新的蛋白質
CREB2,可抑制 CREB 的作用,而阻礙短期記憶轉換成長期記憶。由於
CREB2 的發現,CREB 現在改稱為 CREB1。所以長期記憶的形成,除了需要
CREB1 的製造外,還需要將 CREB2 移除掉。
肯德爾除了飲水思源一直還在用海蝸牛做研究外,在 1990 年代還擴展到用較複雜的哺乳類老鼠做實驗,研究有關學習和記憶的基因。他發現腦部海馬突觸的長期改變對空間記憶的儲存很重要。在
1999 年的美國國家科學研究院學報 (Proc Natl Acad Sci USA),肯德爾的研究團隊對年輕和年老的老鼠做迷宮和腦部海馬切片的研究,發現年老空間記憶的衰退和腦部海馬長期增強的後階段 (L-LTP,late phase of long-term potentiation) 減少有關。由於
L-LTP 依賴於 cAMP 的活化,他們發現增強 cAMP 的藥物,例如多巴胺
D1/D5 受體促進劑和 cAMP 磷酸雙脂化酉每抑制劑
rolipram,可降低 L-LTP 的減少和降低空間記憶的衰退。
肯德爾所研究出的學習和記憶在細胞分子層次的作用機制,基本上也適用於人類。所以,我們的記憶可以說是位於突觸。肯德爾精湛的研究除了提供我們對學習和記憶的深層了解外,也提供了開發有關增強記憶藥物的契機。
附文 (1):小字典大學問
亞伯雷斯克獎-美國的諾貝爾獎
(電腦字數統計:中文字
1,107,英數字 31)
亞伯雷斯克獎 (Albert Lasker Award)
素有「美國的諾貝爾獎」盛名,是生物醫學領域最被人垂涎的一個大獎,也是諾貝爾獎的前導。從
1962
年開始頒獎至今,已有一半的亞伯雷斯克獎得主再獲得諾貝爾獎,到
2000 年共有 63 位亞伯雷斯克獎得主獲得諾貝爾獎,而且經常是在得到亞伯雷斯克獎兩年內獲得諾貝爾獎
[例如 1998 年的諾貝爾生理或醫學獎得主佛曲家 (Robert F. Furchgott)
和繆拉德 (Ferid Murad) 是 1996 年的亞伯雷斯克獎得主],其中有
12 位是得了亞伯雷斯克獎後的同一年獲得諾貝爾獎。從 1979
年到 2000 年這 22 年來,除了 1990 和 1991 兩年外,諾貝爾獎得主都有亞伯雷斯克獎得主。亞伯雷斯克獎的得獎研究可以說是近代生物醫學的發展史。
亞伯雷斯克獎是紐約市的慈善家亞伯雷斯克和瑪麗伍德沃 (Mary Woodward)
雷斯克夫婦在 1944 年成立,自 1946
年起每年頒給研究出具發展性和影響深遠的基礎醫學研究的世界最頂尖的精英。除基礎醫學研究和臨床醫學研究二獎外,在
1996
年又加了醫學特別成就獎。這三個獎中又以基礎醫學研究獎最重要、最受重視,因為基礎醫學研究是臨床醫學研究之母,所以再獲得諾貝爾獎的,幾乎全是亞伯雷斯克獎的基礎醫學研究獎得主。
雷斯克基金會的成立是想要喚起大眾了解生物醫學研究對一健康的社會是有巨大的價值。雷斯克夫婦相信科學研究和對基本人類生物學及疾病進程的基本瞭解是延長生命精華和降低疾病折磨的關鍵,所以基金會的建立是要使這個強烈的信仰能永存不朽。雷斯克基金會的任務是要提升和支持醫學研究是一普遍優先重要的事,因而使得國內和國際的政策和資源強力支持於去除威脅生命的疾病和殘障,及改善健康的標準。
除了執行頒獎外,這基金會還企圖創造一個集合點用於教育大眾有關人類健康研究的重要性。所以基金會建立不久便開始一大眾教育的計畫,致力於鼓勵美國聯邦政府對生物醫學研究的財力支持。美國最重要的研究單位
-- 國家健康研究院 (NIH) -- 是這基金會支持下的最大受益者。NIH
資助的研究 (NIH 也資助部分我的博士研究)幫助延長生命的精華,去除折磨日常生活的疾病,增加個人和國家的生產力,及降低不必要疾病和殘障的折磨。
自從亞伯雷斯克在 1953
年逝世後,瑪麗雷斯克接下重擔持續努力,使其在往後 40
年直到 1994
年逝世,成為美國在健康和科學最具影響力的人物之一。
亞伯雷斯克獎和同在紐約市的哥倫比亞大學有深厚關係,頒獎和得獎人的演講常在哥大舉行。記得
1988 年得主之一的切克 (Thomas R. Cech) 是發現 RNA 也具有酉每的催化作用,這和我博士研究主題人造
RNA 酉每有關,我還特別去聽他的演講;結果隔年他就獲得諾貝爾化學獎。瑪麗雷斯克逝世後捐一棟生物醫學研究大樓給哥大,並在
1995 年 10 月 16
日正式使用,這是紐約市第一個醫學研究和生物科技園區的五棟研究大樓之一。
什麼時候有「台灣的諾貝爾獎」?台灣的財團或富翁想要對社會有深遠的貢獻和影響,不妨考慮效法雷斯克夫婦對健康和科學的支持和努力?
附文 (2):精神分裂症
(電腦字數統計:中文字
908,英數字 27)
精神分裂症的英文 schizophrenia,是源自希臘字的「分裂」(split) 和「精神」(mind)。精神分裂症常被誤認為有多重性格,其實精神分裂症指的是和真實分裂,不能分辦什麼是真的,什麼是假的,並沒有多重性格。
精神分裂症是最常見的精神病之一,其發生率比阿滋海默氏症 (Alzheimer's disease)、糖尿病或多發性硬化症 (multiple sclerosis) 還要多,大概每一百人中,有一人有這個病。男女罹患的機率相同,不過男性罹患的高峰期較早,通常在
18-26 歲;女性則在 26-45 歲。精神分裂症的醫療消耗不小,根據美國腦神經學會
1997 年的統計,這個病佔去了美國所有病床的四分之一,一年醫療花費
$3,250 億美元。
精神分裂症的症狀有如:(1) 妄想- - 奇怪、錯誤的信念,例如認為被外星人控制、有人要捉拿他等。(2) 幻覺
-- 聽到奇怪的聲音、看到奇怪的東西、聞到奇怪的味道、感覺到奇怪的感覺(例如有虫在皮膚內爬)等。(3) 不正常、沒組織的想法或(和)語言
-- 少說話,說話沒組織,中途立意換話題等。(4) 工作和社交能力崩潰。(5) 緊張症。
精神分裂症病人一個普遍的現象是有較大的側腦室 (lateral ventricles)。此外,還有些病人腦部有較小的海馬 (hippocampus)、較大的基底神經節、和額葉前剖皮質異常;不過這些現象也會發生在沒有精神分裂症的人。
精神分裂症的原因還不完全清楚,可能是由多種因子造成的。除了多巴胺的過度反應外,基因是一個危險因子。一般人口,如前述的只有
1% 有精神分裂症;而兄弟姊妹有精神分裂症的人,則增為有
15% 也會罹患。同卵雙胞胎同時有此症的機率約 50%;而異卵雙胞胎則只有約
15%。
環境也是一個危險因子,例如家庭壓力、社交互動不良、幼年感染病毒或創傷等,都可能誘發精神分裂症。
治療精神分裂症的一些精神病藥物(例如在 1950 年代就存在的第一個治療精神病的藥物
chlorpromazine,其長相請見圖三)的作用機制類似多巴胺,可以和多巴胺受體結合,因而阻擋多巴胺和多巴胺受體結合,所以可以降低多巴胺在突觸的傳導,而降低多巴胺的過度反應。
由於這些精神病藥物可降低多巴胺的傳導,所以也可能產生一些類似巴金森氏症的副作用。其他可能的副作用包括肌緊張度不足、坐立不安、遲緩性運動困難(臉、嘴和身體的不自主性異常動作)、體重增加、皮膚問題等。
此外,高劑量的安非他命類物質會增加多巴胺(和其他神經傳導因子)的過度反應,也會引起類似精神分裂症的症狀,這個叫做「安非他命精神病」(amphetamine psychosis),會進一步惡化精神分裂症。所以安非他命千萬碰不得。
附文 (3):注意力不足活動過度症 (ADHD)
(電腦字數統計:中文字
442,英數字 19)
注意力不足活動過度症 (ADHD, attention deficit hyperactivity disorder) 也是一個和多巴胺有關連的病症。雖然其病因還不清楚,一般認為和腦部多巴胺的活性不足有關。
在美國所有的學齡兒童中有約 5% 男孩和 2% 女孩有此症,也就是約
150-350 萬學齡兒童。有此症的兒童長大成人後,最多可高達
60% 的人還會有此症。
Ritaline (化學俗名 methylphenidate hydrochloride,圖四)
最初是在 1950 年代用於治療嗜眠病(在不規律時間突然睡著),在美國目前則是治療此症最熱門的藥物;在過去八年來,ritaline
的生產增加了七倍;大概有 100 萬兒童靠藥物治療,一年花費約
30 億美元。
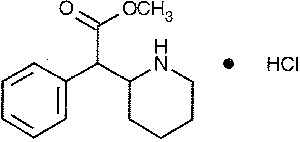
圖四:Ritaline (化學俗名 methylphenidate hydrochloride)
Ritaline 可以降低多巴胺的再吸收,使腦部有較多的多巴胺可利用,多巴胺也就可以留在突觸久一點,所以可以降低活動過度和其他的行為問題。Ritaline
可能的副作用包括睡不著、刺激過敏、食慾降低、憂鬱、性格改變等。
此外,ritaline 在腦部的作用十分類似古柯鹼,所以藥物成癮或可能增加兒童長大後較容易吃毒品的風險,是一個受重視的爭議性問題。動物研究顯示,在幼年時有受過這方面刺激的動物,較容易有吃古柯鹼的傾向。另外,有些研究顯示,ritaline
使人較有吃毒品成癮的傾向。不過有些研究人員認為,有注意力不足活動過度症 (ADHD) 的兒童,長大後本身就有較容易使用各種藥物的傾向。
附文 (4):杭亭頓氏病 (Huntington's disease)
(電腦字數統計:中文字
227,英數字 12)
杭亭頓氏病也稱為杭亭頓氏舞蹈病 (Huntington's chorea),是一種遺傳病,有此病者所生育的下一代有
50% 的機率會遺傳到。杭亭頓氏病的基因在第四號染色體的短臂,基因檢驗可以知道是否有遺傳到突變基因。
杭亭頓氏病通常在中年(35-50 歲)開始,一般病發後 13-15 年內會死亡,死因經常是肺炎或致命性的跌倒。其症狀包括痙攣、抽筋、腦細胞逐漸消失、舞蹈、運動失調、心智障礙等。腦部的神經傳導因子
g-胺丁酸 (GABA) 和 P 物質會降低;不過補充
g-胺丁酸的治療並無效。杭亭頓氏病目前沒有有效的治療方法,舞蹈和騷動可用精神病藥物 (如
chlormazine) 或利血平 (reserpine) 來壓抑。
(Written on 10/17/2000.)
© Copyright 2000-2002 DEENG-LIH HUANG. All rights reserved.
![]() Posted
on 01/02/2002.
Posted
on 01/02/2002.
相關文章:
![]() Disclaimer: 本文版權為作者所有。文章內容是作者的責任,本網站或健康族股份有限公司和文章內容無關聯並對文章內容不負責任。Copyright of this article belongs to the author. The content of the article is the responsibility of the author. This web site or Health Family Corporation have no correlation with the content of this article and have no responsibility over the content of this article.
Disclaimer: 本文版權為作者所有。文章內容是作者的責任,本網站或健康族股份有限公司和文章內容無關聯並對文章內容不負責任。Copyright of this article belongs to the author. The content of the article is the responsibility of the author. This web site or Health Family Corporation have no correlation with the content of this article and have no responsibility over the content of this article.
© 2001-2002 健康族股份有限公司。保留所有權利。所有資訊僅打算供一般知識參考,並不打算診斷、治療、治癒或防止任何疾病或取代任何醫療指示。有任何健康問題,請一定要儘速求醫。要開始一個新的健康療法時,請一定要先咨詢健康醫療專業人員。
© 2001 HEALTH FAMILY CORPORATION. All rights reserved. All
information is intended for reference of general knowledge only and is not
intended to diagnose, treat, cure or prevent any disease or to substitute
for a medical advice. Please make sure to seek prompt medical care for any
specific health problems. Please make sure to consult a health medical
professional before starting a new fitness regimen.